HLA-B*57:01
Codi: 71832
Tipus: Estudis d’HLA relacionats amb malalties i infertilitat
Informació tècnica
Utilitat
La determinació de l’al·lel HLA B*57:01 ens permet identificar pacients amb alta probabilitat de desenvolupar hipersensibilitat al tractament amb Abacavir.
Mètode
Tipificació de l’antigen B*57 mitjançant PCR a temps real o PCR-SSO i tipificació HLA-B d’alta resolució mitjançant PCR-NGS o SBT.
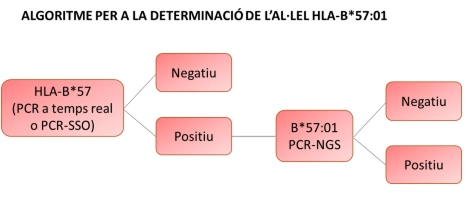
Algoritme diagnòstic
Seguint l’algoritme diagnòstic, si el resultat de la PCR a temps real o la PCR-SSO és B*57 positiu es procedeix a realitzar la PCR-NGS o SBT per determinar si és B*57:01.
Resultats
- En la tipificació de l’antigen B*57 els resultats possibles són: B*57 negatiu o B*57 positiu.
- En la tipificació HLA-B d’alta resolució els resultats possibles són: B*57:01 negatiu o B*57:01 positiu.
Precaucions
No aplica.
Temps de resposta
15 dies.
Informació sobre l’espècimen
Mostra: Sang total.
Tub: Tub EDTA K3 4 ml.
Volum mínim: 500µl.
Estabilitat:
- En refrigeració: 2 setmanes.
- A -20ºC: a partir de 2 setmanes.
Instruccions de transport: Preferiblement a temperatura ambient.
Motiu de rebuig: Mostra coagulada.
Informació administrativa
Codi BST: 71832.
Codi BST antic: LRD2056.
Descripció de la prova: HLA-B*57:01.
Sinònims: No aplica.
Secció: Histocompatibilitat i Immunogenètica.
Tarifa BST: Consultar les tarifes actualitzades.
Perfils
No aplica.
Referències
- Manual dels “Standards for Histocompatibility Testing” de l’EFI (darrera versió).